Задание 4 Параграф 20 ГДЗ Рабочая тетрадь Габриелян Остроумов 8 класс (Химия)
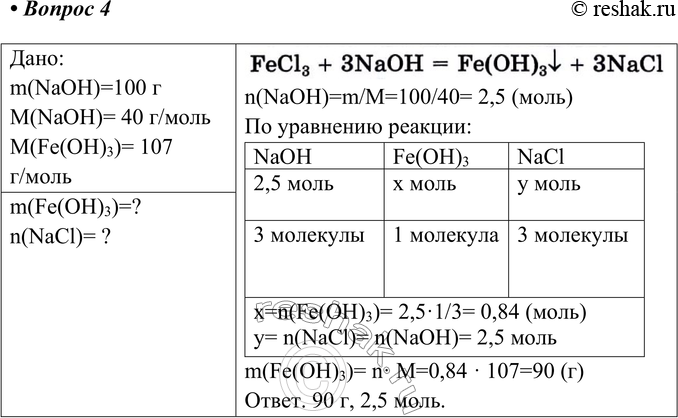
4. Рассчитайте массу осадка в реакции обмена между раствором хлорида железа(ІІІ) и 100 г гидроксида натрия и количество вещества хлорида натрия.
Ниже вариант решения задания из учебника Габриелян, Остроумов, Сладков 8 класс, Просвещение:
4. Рассчитайте массу осадка в реакции обмена между раствором хлорида железа(ІІІ) и 100 г гидроксида натрия и количество вещества хлорида натрия.
Дано:
Решение:
FeCl3 + 3NaOH = Fe(OH)3v + 3NaCl
Дано:
m(NaOH)=100 г
M(NaOH)= 40 г/моль
M(Fe(OH)3)= 107 г/моль
n(NaOH)=m/M=100/40= 2,5 (моль)
По уравнению реакции:
NaOH Fe(OH)3 NaCl
2,5 моль x моль y моль
3 молекулы 1 молекула 3 молекулы
x=n(Fe(OH)3)= 2,5·1/3= 0,84 (моль)
y= n(NaCl)= n(NaOH)= 2,5 моль
m(Fe(OH)3)= n· M=0,84 · 107=90 (г)
Ответ. 90 г, 2,5 моль.
