Часть l Параграф 17 ГДЗ Рабочая тетрадь Габриелян Остроумов 9 класс (Химия)
§ 17. Аммиак Часть I 1. Молекулярная формула аммиака а) Электронная формула аммиака: б) Структурная формула аммиака: Геометрическая форма молекулы с обозначением атомов и частичных зарядов:


Ниже вариант решения задания из учебника Габриелян, Остроумов, Сладков 9 класс, Просвещение:
§ 17. Аммиак
Часть I
1. Молекулярная формула аммиака
а) Электронная формула аммиака:
б) Структурная формула аммиака:
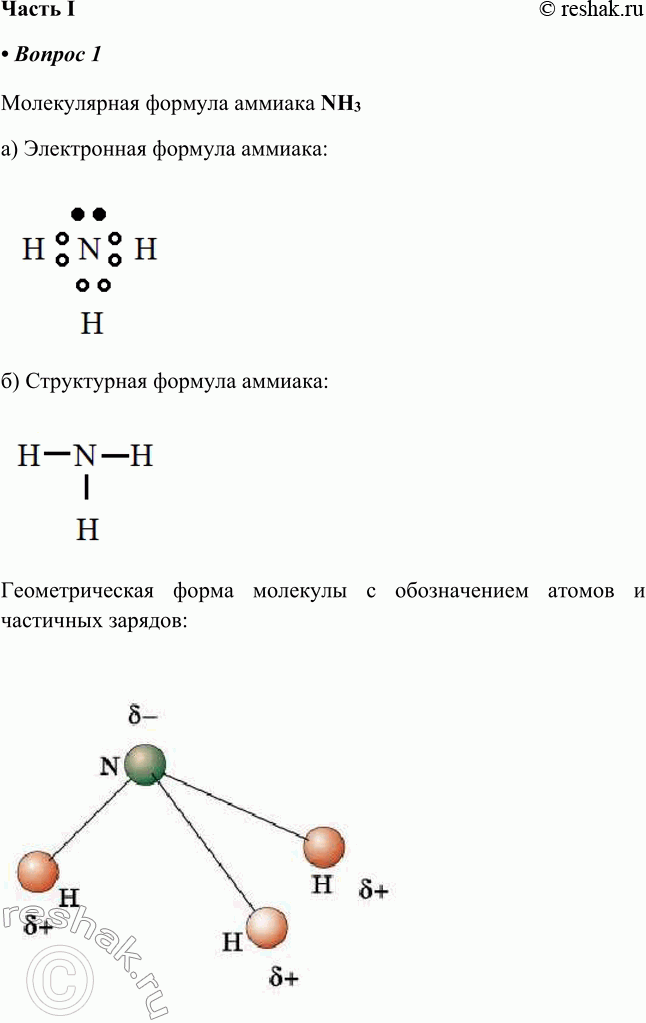
Геометрическая форма молекулы с обозначением атомов и частичных зарядов:
Молекулярная формула аммиака NH3
а) Электронная формула аммиака
б) Структурная формула аммиака
Геометрическая форма молекулы с обозначением атомов и частичных зарядов:
2. Физические свойства аммиака.
Физические свойства аммиака:
А) бесцветный газ
Б) резкий характерный запах
В) хорошо растворяется в воде
Г) D(возд.) = M(NH3)/M(возд.)= 17 / 29 = 0,59, поэтому аммиак собирают в сосуд дном вверх.
3. Химические свойства аммиака.
1) За счёт атома азота проявляет сильные _ свойства.
Дополните схемы реакций и расставьте в них коэффициенты с помощью метода электронного баланса.
а) NH3 + О2 = N2 + __
б) NH3 + О2 = NO + __
2) За счёт _ механизма образуется катион _
За счёт этого же механизма при взаимодействии аммиака с кислотами образуются соли:
a) NH3 + НСд = __________
6) NH3 + H2SO4 = _ NH3 + H2SO4 =
(средняя соль) (кислая соль)
в) NH, + H,PO. = _ NH, + НяР04 =
(средняя соль) (кислая соль)
NH3 + Н3РО4 =
(кислая соль)
3) С водой образует гидрат аммиака NH3 • Н20, который диссоциирует:
Химические свойства аммиака.
1) За счёт атома азота проявляет сильные ВОССТАНОВИТЕЛЬНЫЕ свойства.
2) За счет ДОНОРНО-АКЦЕПТОРНОГО механизма образуется катион аммония NH4+
А) NH3 + HCl > NH4Cl
Б) 2NH3 + H2SO4 > (NH4)2SO4 (средняя соль)
NH3 + H2SO4 > NH4HSO4 (кислая соль)
В) 3NH3 + H3PO4 > (NH4)3PO4 (средняя соль)
NH3 + H3PO4 > NH4H2PO4 (кислая соль)
2NH3 + H3PO4 > (NH4)2HPO4 (кислая соль)
3) NH3· H2O > NH4+ + OH-
4. Получение аммиака.
а) В лаборатории: ________________________________________
б) В промышленности:______________________________________
Получение аммиака.
а) В лаборатории:
2NH4Cl + Ca(OH)2 > 2NH3 + 2H2O + CaCl2
б) В промышленности: N2 + 3H2 2NH3
5. Заполните таблицу.
Распознавание аммиака
Способ распознавания
Аналитический эффект
а) Обнаружение запаха
б) Влажная лакмусовая бумага
в) Стеклянная палочка, смоченная НСl
Аналитический эффект
Резкий характерный запах
Синеет
Дымится
