Часть l Параграф 12 ГДЗ Рабочая тетрадь Габриелян Остроумов 9 класс (Химия)
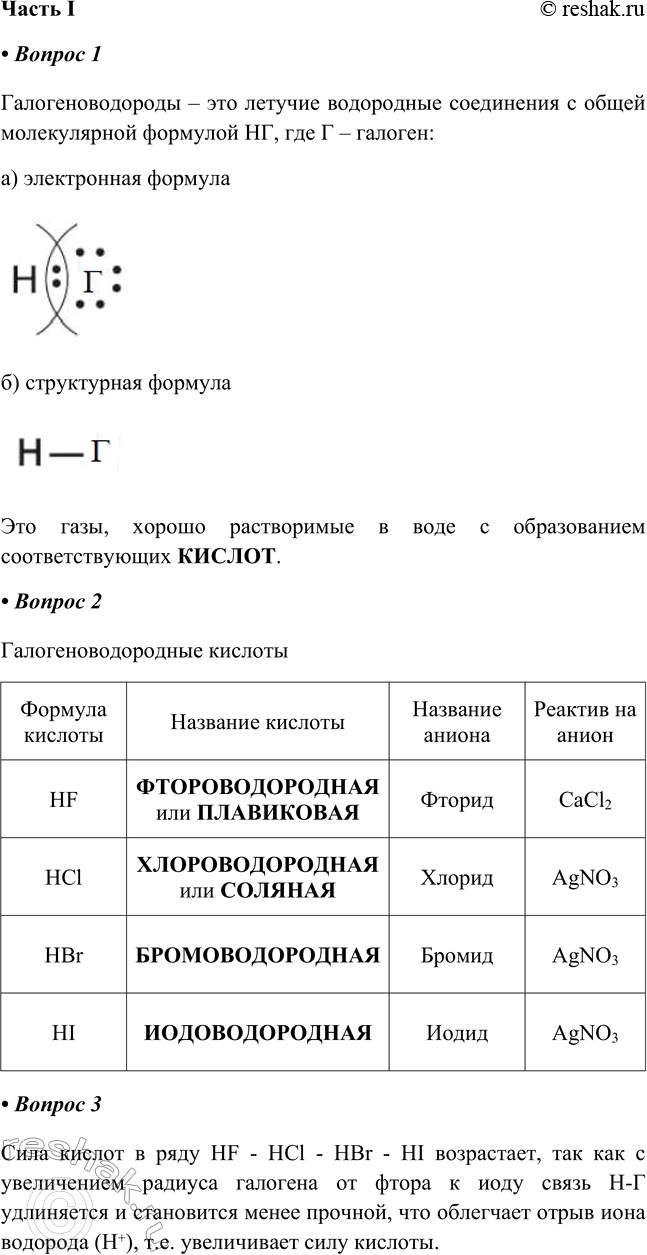
§ 12. Соединения галогенов Часть I 1. Галогеноводороды — это _ с общей молекулярной формулой НГ, где Г — галоген: а) электронная формула______________ б) структурная формула ______________ Это газы, хорошо растворимые в воде с образованием соответствующих ____ Галогеноводороды – это летучие водородные соединения с общей молекулярной формулой НГ, где Г – галоген:
Ниже вариант решения задания из учебника Габриелян, Остроумов, Сладков 9 класс, Просвещение:
§ 12. Соединения галогенов
Часть I
1. Галогеноводороды — это _ с общей молекулярной формулой НГ, где Г — галоген:
а) электронная формула______________
б) структурная формула ______________
Это газы, хорошо растворимые в воде с образованием соответствующих ____
Галогеноводороды – это летучие водородные соединения с общей молекулярной формулой НГ, где Г – галоген:
а) электронная формула
б) структурная формула
Это газы, хорошо растворимые в воде с образованием соответствующих КИСЛОТ.
2. Заполните таблицу.
Галогеноводородные кислоты
Формула
кислоты
Название кислоты
Название
аниона
Реактив на анион
3. Сила кислот в ряду HF, НСl, HBr, HI _____, ____ так как ____
Сила кислот в ряду HF - HCl - HBr - HI возрастает, так как с увеличением радиуса галогена от фтора к иоду связь H-Г удлиняется и становится менее прочной, что облегчает отрыв иона водорода (H+), т.е. увеличивает силу кислоты.
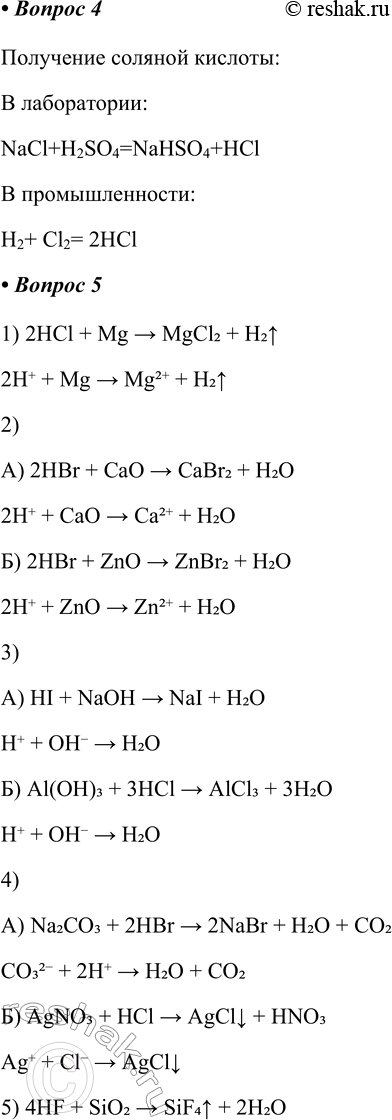
4. Получение соляной кислоты:
а) в промышленности
б) в лаборатории
Получение соляной кислоты:
В лаборатории:
NaCl+H2SO4=NaHSO4+HCl
В промышленности:
H2+ Cl2= 2HCl
5. Растворы галогеноводородов проявляют свойства, типичные для кислот. Напишите в молекулярной и ионной форме уравнения реакций растворов галогеноводородов:
1) с металлами:
2) с основными и амфотерными оксидами:
3) с основаниями и амфотерными гидроксидами:
4) с солями с образованием газа (^) или осадка (v):
5) HF взаимодействует с SiO2
1) 2HCl + Mg > MgCl2 + H2^
2H+ + Mg > Mg2+ + H2^
2)
А) 2HBr + CaO > CaBr2 + H2O
2H+ + CaO > Ca2+ + H2O
Б) 2HBr + ZnO > ZnBr2 + H2O
2H+ + ZnO > Zn2+ + H2O
3)
А) HI + NaOH > NaI + H2O
H+ + OH- > H2O
Б) Al(OH)3 + 3HCl > AlCl3 + 3H2O
H+ + OH- > H2O
4)
А) Na2CO3 + 2HBr > 2NaBr + H2O + CO2
CO32- + 2H+ > H2O + CO2
Б) AgNO3 + HCl > AgClv + HNO3
Ag+ + Cl- > AgClv
5) 4HF + SiO2 > SiF4^ + 2H2O
